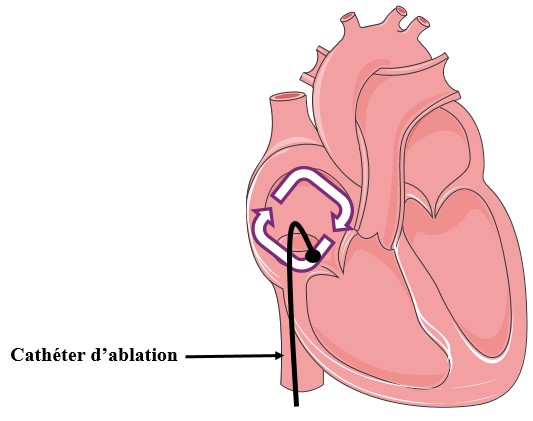
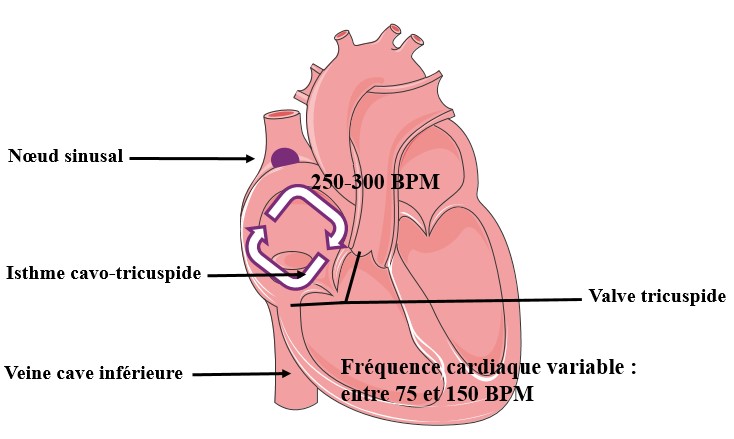
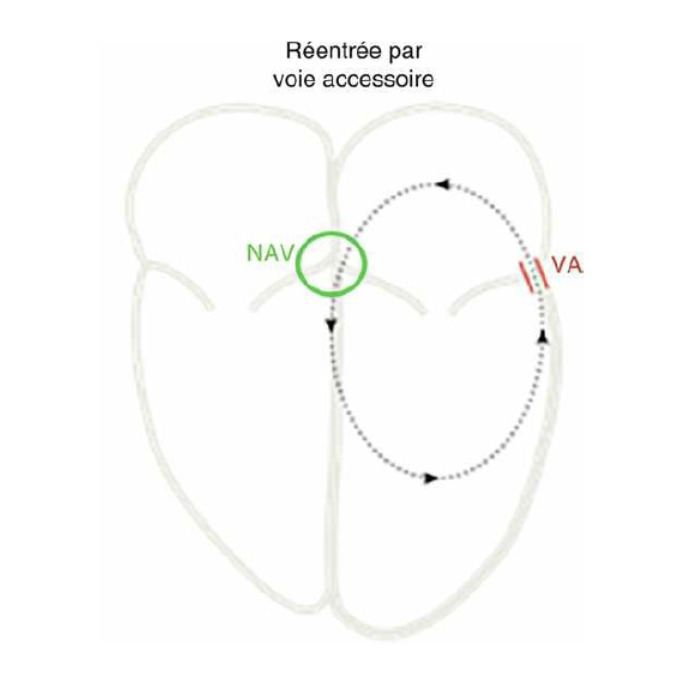
L’ablation par cathéter des arythmies cardiaques est une procédure médicale minimement invasive utilisée pour traiter certains types d’arythmies, ou irrégularités du rythme cardiaque. Durant cette procédure, un cathéter fin et flexible est inséré dans une veine, généralement au niveau de l’aine, et guidé jusqu’au cœur. Des électrodes à l’extrémité du cathéter permettent de localiser précisément la zone du cœur générant l’arythmie. Une fois cette zone identifiée, elle est détruite (ou « ablatée ») en utilisant une des différentes formes d’énergie, comme la radiofréquence ou le froid. Cette technique vise à interrompre les signaux électriques anormaux dans le cœur pour restaurer un rythme cardiaque normal. L’ablation par cathéter ne signifie pas que l’on « enlève » quelque chose. Il ne s’agit pas d’une chirurgie cardiaque, la cage thoracique n’est pas ouverte. L’intervention est pratiquée par le cardiologue spécialisé en rythmologie interventionnelle. Les ablations par cathéter constituent désormais le traitement de référence pour la majorité des arythmies cardiaques.
Ces interventions complexes nécessitent des ressources importantes et sont typiquement réalisées dans notre centre.